9EF - Atividades de avaliação
+++++++++++++++++++++
7EF
Saída - Trilha Pedra Branca - São José - SC - 09/07/2016
Descrição da Atividade
Início às 08h00min horas da manhã do sábado, com um intervalo de 20 minutos para um lanche e término às 12 horas. Os 19 alunos presentes foram acompanhados por 4 professores e 2 mães de alunos.
As normas de condutas: cuidados com resíduos, não provocar danos ao ambiente, comportamento, atenção às tarefas, cumprimento dos prazos...
As atividades a serem desenvolvidas na trilha do morro Pedra Branca, referentes ao conteúdo de Ciências/Biologia, incluem:
- Trilhas dos sentidos: nessa atividade foram abordados assuntos e experiências referentes à percepção do espaço com o uso dos sentidos na observação da mata e seu entorno; descrição de todos os sons percebidos no raio de alcance da sua capacidade auditiva; descrição dos diferentes aromas sentidos na mata. O que mais chama a atenção no local?
- Mostrar as características, peculiaridades, e a importância dessa vegetação para o clima local e da cidade, e como a quebra desse equilíbrio pode trazer consequências desastrosas para a população, citando as consequências do desmatamento, erosão, efeito estufa e outras.
- Observar as influências de vários fatores (relevo, clima, regime de chuvas) na determinação do tipo de formação vegetal e sua distribuição.
- Destacar os aspectos morfológicos das plantas ali encontradas, identificando as briófitas, pteridófitas, gimnospermas e angiospermas.
- Observar e registrar a diversidade da fauna, especialmente insetos e aves.
- Para finalizar a tarefa, foi solicitada uma pesquisa de aprofundamento sobre a importância dos vegetais na manutenção do clima de uma região.
- Verificar as adaptações ao ambiente.
- Observar a vegetação de Mata Úmida.
- Discutir a importância ambiental nos ambientes de mata atlântica.
- Registrar os sinais de influência do homem no local.
====================================
9EF
- ANÁLISE OU DECOMPOSIÇÃO – é a reação onde uma substância se divide em duas ou mais substâncias de estrutura mais simples.
- SIMPLES TROCA OU DESLOCAMENTO – é a reação onde uma substância simples troca de lugar com um elemento de uma substância composta, se transformando em uma nova substância simples.
Exemplos:
Zn + H2SO4 → ZnSO4 + H2
- DUPLA TROCA – é a reação onde duas substâncias compostas reagem e trocam seus elementos, se transformando em duas substâncias também compostas.
Exemplos:
HCl + NaOH → NaCl + H2O
=======================================
Massa Atômica de um Átomo
A massa atômica de determinado elemento químico indica quantas vezes ela é maior que a massa de 1 u ou 1/12 da massa de um átomo de carbono 12.
“A massa atômica de um átomo é a sua massa determinada em unidades de massa atômica (u), sendo que 1 u é igual a 1/12 da massa de 1 átomo de carbono 12.”
Essa definição pode parecer um tanto complicada quando se lê inicialmente, mas ao longo deste texto você verá que é bem simples.
Para começar, pense em quando você vai a um supermercado comprar arroz. Geralmente, você compra sacos de 2 kg ou de 5 kg, não é mesmo?! Esse exemplo serve para mostrar que a massa de um corpo é determinada através da comparação com uma unidade-padrão conveniente. No caso do saco de arroz, a unidade escolhida para servir de padrão de comparação foi o quilograma (kg).
O quilograma-padrão equivale a um cilindro de 3,917 cm de altura e de diâmetro, feito de 10% de irídio e 90% de platina. Ele fica guardado no interior de três cúpulas de vidro na sede do Bureau Internacional de Pesos e Medidas, na cidade de Sèvre, França.
Assim, quando se diz que um saco de arroz tem 5 kg, isso quer dizer que a sua massa é cinco vezes maior que a massa de 1 quilograma. No entanto, se fosse para falar da massa de uma formiga, você não usaria o kg, pois a massa de uma formiga é muito menor que a massa do quilograma-padrão. Isso significa que é importante escolher padrões convenientes para determinar cada medida específica.

Ilustração de relação entre a massa de um pacote de arroz e o quilograma-padrão
Isso se aplica à massa atômica ou massa dos átomos. É impossível pesar um átomo em uma balança e dizer a sua massa, pois os átomos são tão pequenos que nem mesmo os microscópios mais modernos conseguem enxergá-los.
Por isso, os cientistas decidiram escolher como padrão de medida da massa atômica a massa de um átomo específico. Atualmente, o carbono 12 é o átomo que serve como referência para a determinação da massa dos outros átomos.
A massa atômica do carbono 12 é exatamente 12 u. Assim, 1 u (uma unidade de massa atômica) é igual a 1/12 da massa do carbono 12.
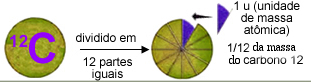
A unidade de massa atômica é 1/12 da massa do carbono 12
Por isso, podemos dizer que a massa atômica, expressa em u, indica quanto a massa de 1 átomo de certo elemento químico é maior que a massa de 1 u. Sabe-se que 1 u é igual a 1,66054 . 10-24 g.
Por exemplo, o hidrogênio possui três isótopos diferentes na natureza, e o mais comum deles é o 1H. A massa atômica do 1H é igual a 1 u (valor arredondado), o que quer dizer que a massa de 1 átomo de hidrogênio é exatamente igual a 1/12 da massa do carbono 12.
Por outro lado, a massa do isótopo mais comum do hélio é 4 u, o que quer dizer que a massa do átomo de hélio é quatro vezes maior que a massa de 1/12 do carbono 12.
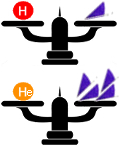
Massas atômicas do hidrogênio e do hélio em comparação com 1 unidade de massa atômica (1/12 da massa do carbono 12)
Hoje as massas atômicas dos átomos são normalmente medidas por meio de um aparelho chamado de espectrômetro de massa.
No Ensino Médio, costumamos usar os valores das massas atômicas de forma arredondada. Por exemplo, a massa atômica do isótopo principal do hélio é, na realidade, 4,00030 u, mas usamos somente 4 u. Ao fazer isso, vemos que o valor da massa atômica fica exatamente igual ao número de massa (A) do átomo, que é a soma dos prótons e dos nêutrons que existem no núcleo atômico. Veja como isso ocorre no caso do hélio: ele possui dois prótons e dois nêutrons no núcleo, portanto, seu número de massa é igual a 4.
Na Tabela Periódica, costumam aparecer abaixo do símbolo de cada elemento as respectivas massas atômicas. Porém, esses valores não são a massa atômica de um átomo, mas sim a massa atômica de um elemento.
Fonte: Mundo Educação
========================================
Substâncias e misturas
+++++++++++++++++++++
7EF
Saída - Trilha Pedra Branca - São José - SC - 09/07/2016
Descrição da Atividade
Início às 08h00min horas da manhã do sábado, com um intervalo de 20 minutos para um lanche e término às 12 horas. Os 19 alunos presentes foram acompanhados por 4 professores e 2 mães de alunos.
As normas de condutas: cuidados com resíduos, não provocar danos ao ambiente, comportamento, atenção às tarefas, cumprimento dos prazos...
As atividades a serem desenvolvidas na trilha do morro Pedra Branca, referentes ao conteúdo de Ciências/Biologia, incluem:
- Trilhas dos sentidos: nessa atividade foram abordados assuntos e experiências referentes à percepção do espaço com o uso dos sentidos na observação da mata e seu entorno; descrição de todos os sons percebidos no raio de alcance da sua capacidade auditiva; descrição dos diferentes aromas sentidos na mata. O que mais chama a atenção no local?
- Mostrar as características, peculiaridades, e a importância dessa vegetação para o clima local e da cidade, e como a quebra desse equilíbrio pode trazer consequências desastrosas para a população, citando as consequências do desmatamento, erosão, efeito estufa e outras.
- Observar as influências de vários fatores (relevo, clima, regime de chuvas) na determinação do tipo de formação vegetal e sua distribuição.
- Destacar os aspectos morfológicos das plantas ali encontradas, identificando as briófitas, pteridófitas, gimnospermas e angiospermas.
- Observar e registrar a diversidade da fauna, especialmente insetos e aves.
- Para finalizar a tarefa, foi solicitada uma pesquisa de aprofundamento sobre a importância dos vegetais na manutenção do clima de uma região.
- Verificar as adaptações ao ambiente.
- Observar a vegetação de Mata Úmida.
- Discutir a importância ambiental nos ambientes de mata atlântica.
- Registrar os sinais de influência do homem no local.
====================================
9EF
REAÇÕES QUÍMICAS
As substâncias podem
combinar-se com outras substâncias transformando-se em novas substâncias. Para
estas transformações damos o nome de Reações Químicas.
Reação
Química é um fenômeno onde os átomos permanecem intactos. Durante as reações,
as moléculas iniciais são "desmontadas" e os seus átomos são
reaproveitados para "montar" novas moléculas.
No
nosso cotidiano, há muitas reações químicas envolvidas, como por exemplo, no
preparo de alimentos, a própria digestão destes alimentos no nosso organismo, a
combustão nos automóveis, o aparecimento da ferrugem, a fabricação de remédios,
etc.
EQUAÇÃO QUÍMICA
A forma que representamos a
reação química chama-se Equação Química.
Equação Química – é a representação gráfica da reação
química.
Nela colocamos os elementos
que estão envolvidos na reação, de forma abreviada, e como ela aconteceu,
através de símbolos já padronizados.
As Equações Químicas
representam a escrita usada pelos químicos e de forma universal, ou seja, é a
mesma em qualquer país.
As substâncias que
participam da reação química são chamadas de produtos ou reagentes na equação
química.
Reagentes (1° membro) – são as substâncias que
estão no início da reação. São as que irão reagir, sofrer a transformação.
Produtos (2° membro) – são as substâncias
resultantes da reação química.
Exemplo: Duas
moléculas de gás hidrogênio juntam-se com uma molécula de gás oxigênio formando
duas moléculas de água.
2H2 +
O2 → 2 H2O
reagente
produto
Observe que o H2 e
o O2 são reagentes e H2O
é o produto.
Para representar a reação
química, utiliza-se uma seta apontando para o lado direito, indicando a
transformação.
Em cima da seta, são
utilizados alguns símbolos indicando as condições nas quais a reação deve ocorrer.
∆ - calor
aq – aquoso (
em água)
cat –
catalisador
λ – energia
luminosa
Em cada substância pode
haver os seguintes símbolos:
↑ -
desprendimento de gás
↓ -
precipitação de um sólido
Nas equações químicas, as
substâncias podem aparecer com seus estados físicos:
(s) – sólido
(l) – líquido
(g) – gasoso
Exemplo:
C (s) + O2 (g) → CO2 (g)
C (s) + O2 (g) → CO2 (g)
BALANCEAMENTO DE
EQUAÇÕES QUÍMICAS
Em uma reação química, a estrutura dos átomos,
enquanto elementos químicos ficam inalterados. Os átomos de um elemento não se
transformam em átomos de outro elemento. Também não há perda ou criação de
átomos novos (Lei de Lavoisier).
O número de átomos dos reagentes deve ser igual ao
número de átomos dos produtos. Quando isso acontece, dizemos que a equação
química está balanceada.
Exemplo de equação balanceada: C + O2
→ CO2
Exemplo de equação química não balanceada: H2
+ O2 → H2O
Observe que na 1ª equação há um carbono e no reagente
e um carbono no produto. Também há dois oxigênios no reagente e dois no produto.
A equação está corretamente balanceada.
Na 2ª equação, há dois hidrogênios no reagente e dois
hidrogênios no produto, porém há dois oxigênios no reagente e apenas um no
produto. Então, deve-se balancear esta equação. Há alguns métodos para balancear
uma equação química. O mais fácil e simples é o Método das
Tentativas.
Para balancear a 2ª equação, podemos colocar o número
2 na frente do H2 e o
número 2 na frente da H2O, assim:
2 H2
+ O2 →
2 H2O
O número de átomos, por exemplo, deve ser mantido
sempre. Para esse número damos o nome de índice. O número que poderá ser
colocado na frente do átomo é o coeficiente, no caso, também 2.
Então temos agora 4 H no reagente e 4 H no produto. Também 2 O no reagente e 2 O no produto. A reação agora está balanceada.
Então temos agora 4 H no reagente e 4 H no produto. Também 2 O no reagente e 2 O no produto. A reação agora está balanceada.
Quando o coeficiente for 1, ele não precisa ser
escrito.
VELOCIDADE DAS REAÇÕES
As reações químicas não
ocorrem com a mesma velocidade: umas são mais rápidas, outras são bem lentas. A
reação entre bicarbonato de sódio, por exemplo, e vinagre, é rápida. Basta os
reagentes entrarem em contato para que ela ocorra. Já a reação que ocorre entre
ferro, oxigênio e água, formando a ferrugem, é lenta.
Alguns fatores podem alterar
a velocidade das reações químicas.
Numa reação entre um comprimido
efervescente e água podemos acelerar a velocidade desta reação. Basta dividir o
comprimido em pedaços iguais. Então quanto mais triturado, mais dividido, mais
rápida é a reação. Este fator é a superfície de contato, que aumenta e faz com
que a reação seja mais rápida.
O mesmo acontece quanto à
temperatura. Se colocarmos o comprimido efervescente em água fria e outro em
água quente, observaremos que com a água quente a reação ocorre mais rápida.
Então, o aumento da temperatura faz com que a velocidade da reação química
aumente.
TIPOS DE REAÇÕES QUÍMICAS
As reações químicas são
classificadas em quatro tipos:
- síntese ou
adição
- análise ou
decomposição
- simples
troca ou deslocamento
- dupla troca
- SÍNTESE OU ADIÇÃO – é a reação onde
duas ou mais substâncias reagem para se transformar em uma. Exemplos:
C + O2
→ CO2
CaO + H2O
→ Ca(OH)2
- ANÁLISE OU DECOMPOSIÇÃO – é a reação onde uma substância se divide em duas ou mais substâncias de estrutura mais simples.
Exemplos:
2AgBr → 2Ag + Br2
2AgBr → 2Ag + Br2
2Cu(NO3)2 → 2CuO +
4NO2 + O2
- SIMPLES TROCA OU DESLOCAMENTO – é a reação onde uma substância simples troca de lugar com um elemento de uma substância composta, se transformando em uma nova substância simples.
Exemplos:
Zn + H2SO4 → ZnSO4 + H2
Fe
+ CuSO4 →
FeSO4 + Cu
- DUPLA TROCA – é a reação onde duas substâncias compostas reagem e trocam seus elementos, se transformando em duas substâncias também compostas.
Exemplos:
HCl + NaOH → NaCl + H2O
FeS
+ 2HCl →
FeCl2 + H2S
LEI DE LAVOISIER
“Numa reação
química, a soma das massas dos reagentes é igual à soma das massas dos
produtos.”
Segundo esta lei, num
sistema químico fechado, qualquer que seja a transformação ocorrida, a massa
segue constante.
Estas afirmativas obedecem a
uma Lei da natureza. Descoberta pelo cientista francês Antoine Lavoisier, no
final do século XVII. Por este motivo, esta lei ficou conhecida como Lei de
Lavoisier ou Lei da Conservação da Massa.
É dele também a célebre
frase: "Na natureza nada se perde,
nada se cria. Tudo se transforma".
Observe:
Uma reação
entre as substâncias A e B transformam-se em C.
A massa da
substância A é 20g e de B é 5g. Qual a massa de C?
A +
B → C
20g 5g x
20g 5g x
Então: 20 + 5 = 25g de C
A +
B → C
20g 5g 25g
20g 5g 25g
Esta reação obedece a Lei de
Lavoisier, onde a soma das massas dos reagentes é igual a soma da massa dos
produtos.
LEI DE PROUST
"Uma determinada substância composta é
formada por substâncias mais simples, unidas sempre na mesma proporção em massa".
O químico francês Joseph
Louis Proust observou que em uma reação química a relação entre as massas das
substâncias participantes é sempre constante. A Lei de Proust ou a Lei das
proporções definidas diz que dois ou mais elementos ao se combinarem para
formar substâncias, conservam entre si proporções definidas.
Observe: A massa de uma
molécula de água é 18g e é resultado da soma das massas atômicas do hidrogênio
e do oxigênio.
H2 –
massa atômica = 1 → 2 x 1 =
2g
O – massa atômica = 16 → 1 x 16 =
16g
Então 18g de água tem sempre
16g de oxigênio e 2g de hidrogênio. A molécula água esta na proporção 1:8.
m H2 = 2g = 1
____
___ __
m O
16g 8
As Leis de Lavoisier e de
Proust são chamadas de Leis Ponderais porque estão relacionadas à massa dos
elementos químicos nas reações químicas.
=======================================
Massa Atômica de um Átomo
A massa atômica de determinado elemento químico indica quantas vezes ela é maior que a massa de 1 u ou 1/12 da massa de um átomo de carbono 12.
“A massa atômica de um átomo é a sua massa determinada em unidades de massa atômica (u), sendo que 1 u é igual a 1/12 da massa de 1 átomo de carbono 12.”
Essa definição pode parecer um tanto complicada quando se lê inicialmente, mas ao longo deste texto você verá que é bem simples.
Para começar, pense em quando você vai a um supermercado comprar arroz. Geralmente, você compra sacos de 2 kg ou de 5 kg, não é mesmo?! Esse exemplo serve para mostrar que a massa de um corpo é determinada através da comparação com uma unidade-padrão conveniente. No caso do saco de arroz, a unidade escolhida para servir de padrão de comparação foi o quilograma (kg).
O quilograma-padrão equivale a um cilindro de 3,917 cm de altura e de diâmetro, feito de 10% de irídio e 90% de platina. Ele fica guardado no interior de três cúpulas de vidro na sede do Bureau Internacional de Pesos e Medidas, na cidade de Sèvre, França.
Assim, quando se diz que um saco de arroz tem 5 kg, isso quer dizer que a sua massa é cinco vezes maior que a massa de 1 quilograma. No entanto, se fosse para falar da massa de uma formiga, você não usaria o kg, pois a massa de uma formiga é muito menor que a massa do quilograma-padrão. Isso significa que é importante escolher padrões convenientes para determinar cada medida específica.

Ilustração de relação entre a massa de um pacote de arroz e o quilograma-padrão
Isso se aplica à massa atômica ou massa dos átomos. É impossível pesar um átomo em uma balança e dizer a sua massa, pois os átomos são tão pequenos que nem mesmo os microscópios mais modernos conseguem enxergá-los.
Por isso, os cientistas decidiram escolher como padrão de medida da massa atômica a massa de um átomo específico. Atualmente, o carbono 12 é o átomo que serve como referência para a determinação da massa dos outros átomos.
A massa atômica do carbono 12 é exatamente 12 u. Assim, 1 u (uma unidade de massa atômica) é igual a 1/12 da massa do carbono 12.

A unidade de massa atômica é 1/12 da massa do carbono 12
Por isso, podemos dizer que a massa atômica, expressa em u, indica quanto a massa de 1 átomo de certo elemento químico é maior que a massa de 1 u. Sabe-se que 1 u é igual a 1,66054 . 10-24 g.
Por exemplo, o hidrogênio possui três isótopos diferentes na natureza, e o mais comum deles é o 1H. A massa atômica do 1H é igual a 1 u (valor arredondado), o que quer dizer que a massa de 1 átomo de hidrogênio é exatamente igual a 1/12 da massa do carbono 12.
Por outro lado, a massa do isótopo mais comum do hélio é 4 u, o que quer dizer que a massa do átomo de hélio é quatro vezes maior que a massa de 1/12 do carbono 12.

Massas atômicas do hidrogênio e do hélio em comparação com 1 unidade de massa atômica (1/12 da massa do carbono 12)
Hoje as massas atômicas dos átomos são normalmente medidas por meio de um aparelho chamado de espectrômetro de massa.
No Ensino Médio, costumamos usar os valores das massas atômicas de forma arredondada. Por exemplo, a massa atômica do isótopo principal do hélio é, na realidade, 4,00030 u, mas usamos somente 4 u. Ao fazer isso, vemos que o valor da massa atômica fica exatamente igual ao número de massa (A) do átomo, que é a soma dos prótons e dos nêutrons que existem no núcleo atômico. Veja como isso ocorre no caso do hélio: ele possui dois prótons e dois nêutrons no núcleo, portanto, seu número de massa é igual a 4.
Na Tabela Periódica, costumam aparecer abaixo do símbolo de cada elemento as respectivas massas atômicas. Porém, esses valores não são a massa atômica de um átomo, mas sim a massa atômica de um elemento.
Fonte: Mundo Educação
========================================
Substâncias e misturas
Substância
química pura apresenta somente
moléculas de um mesmo tipo. Ex.: O2, H2O, C6H12O6.
- Substância
pura simples: formadas por um único tipo de elemento químico. Ex.: O2.
Podem ser classificadas em monoatômicas (H), diatômicas (Cl2),
triatômicas (O3).
- Substância
pura composta: formados por moléculas que apresentam dois ou mais elementos
químicos diferentes em sua composição. Ex.: H2O (binária), C6H12O6
(ternária)
Diferenciamos uma mistura de uma substância pura normalmente através de suas constantes físicas,
tais como: ponto de ebulição (PE), ponto de fusão (PF), densidade (d) e
solubilidade (solub). As substâncias puras mantêm suas constantes durante as
mudanças de estado, diferentemente das misturas. Exemplo:
Água pura: -
PE = 100ºC; PF = 0ºC; d = 1g/cm 3.
Água e sal
de cozinha (NaCl): não apresentam constantes.
Álcool Puro:
PE = 78,5ºC; PF = -177ºC; d = 0,79g/cm 3.
Álcool e
Água: não apresentam constantes.
Mistura é a reunião de duas ou mais substâncias sem que haja reação
química entre elas, e mantendo cada qual suas propriedades. Na mistura de água
e açúcar, não é possível distinguir visualmente um componente do outro: o
açúcar desapareceu na água. Dizemos que essa é uma mistura homogênea. Já na mistura de água e talco, é perfeitamente possível
distinguir visualmente as duas substâncias. Dizemos, então, que essa é uma
mistura heterogênea. A definição de
misturas homogêneas e heterogêneas está ligada ao modo como se percebe a
mistura.
As misturas heterogêneas
apresentam fases distintas. Por
exemplo, uma mistura de água e pedaços de ferro é uma mistura heterogênea em
que se percebem nitidamente duas fases, ou seja, dois componentes distintos: a
água e o ferro. Dizemos então que essa é uma mistura bifásica. Do mesmo modo
falamos em misturas trifásicas, tetrafásicas, etc.
As misturas homogêneas são também
chamadas soluções. Os componentes
(substâncias presentes) de uma solução podem estar nos estados: sólido, líquido
ou gasoso. Podemos dizer que a solução é um tipo de matéria formada por um solvente e um soluto. Soluto é a substância que se encontra dissolvida no
solvente. Solvente é a substância que dissolve o soluto. De acordo com a
quantidade de soluto em relação à de solvente, a solução pode ser:
diluída – pequena quantidade de soluto
concentrada – grande quantidade de soluto
saturada – soluto em quantidade máxima que o
solvente pode dissolver.
Separação dos componentes de uma
mistura
Como os materiais encontrados na
natureza, na sua maioria, são constituídos de misturas de substâncias puras,
para obtê-las, a partir das substâncias compostas é necessário separá-las por
um método adequado. Existem muitos processos para separação de misturas, mas o
método a ser empregado depende das condições materiais para utilizá-lo e do
tipo de mistura a ser separado. Para isso é necessário, em primeiro lugar,
observar se a mistura em questão é homogênea ou heterogênea, para em seguida
escolher o processo mais adequado para separá-la.
Quadro
resumo dos métodos de separação de misturas
Misturas Homogêneas
MÉTODO
|
PROCESSO
|
Destilação Simples (Sólido + Líquido)
|
Por aquecimento, só o líquido entra em ebulição,
vaporiza-se e a seguir condensa-se, separando-se do sólido
|
Destilação Fracionada (Líquido + Líquido)
|
Por aquecimento, os líquidos vaporizam-se e a
seguir condensam-se, à medida que vão sendo atingidos seus pontos de ebulição
|
Líquefação Fracionada (Gás + Gás)
|
Por resfriamento da mistura, os gases se
liqüefazem separadamente, à medida que vão sendo atingidos os seus pontos de
ebulição.
|
Aquecimento Simples (Gás + Líquido)
|
Por aquecimento abaixo do ponto de ebulição do
líquido, ó gás dissolvido é expulso.
|
Misturas
Heterogêneas
MÉTODO
|
PROCESSO
|
Catação (Sólido + Sólido)
|
Os fragmentos são catados com a mão ou pinça
|
Ventilação (Sólido + Sólido)
|
Separação do componente mais leva por corrente de
ar.
|
Levigação (Sólido + Sólido)
|
Separação do componente mais leva por corrente de
água.
|
Dissolução Fracionada (Sólido + Sólido)
|
Separação por meio de um líquido que dissolve
apenas um componente.
|
Separação Magnética (Sólido + Sólido)
|
Apenas um componente é atraído pelo ímã.
|
Fusão Fracionada (Sólido + Sólido)
|
Separação por aquecimento da mistura até a fusão
do componente de menor ponto de fusão.
|
Cristalização Fracionada (Sólido + Líquido)
|
Adiciona-se um líquido que dissolva todos os
sólidos. Por evaporação da solução obtida, os componentes cristalizam-se
separaddamente.
|
Peneiração ou Tamização (Sólido + Sólido)
|
Os componentes estão reduzidos a grãos de diferentes
tamanhos.
|
Sedimentação
|
Separação de duas ou mais camadas devido a
diferentes densidades.
|
Decantação (Sólido + Líquido)
|
Após a sedimentação a fase líquida é escoada.
|
Filtração (Sólido + Líquido)
|
Separa a fase líquida ou gasosa da sólida por
meio de uma superfície porosa.
|
Centrifugação (Sólido + Líquido)
|
Decantação acelerada por uma centrífuga.
|
- Catação: Os grãos ou fragmentos de um
dos componentes são catados com as mãos ou com uma pinça.
- Ventilação: A ventilação é usada para
separar sólidos menos densos, passando-se pela mistura uma corrente de ar que
arrasta o mais leve.
- Levigação: passa-se pela mistura uma
corrente de água e esta arrasta o mais leve.
- Separação magnética: passa-se pela
mistura um imã, se um dos componentes possuírem propriedades magnéticas, será
atraído pelo imã.
- Peneiração: usada quando os grãos que
formam os componentes têm tamanhos diferentes.
- Decantação: usado para separar os
componentes de misturas heterogêneas, constituídas de um componente sólido e
outro líquido ou de dois componentes líquidos, estes líquidos devem ser imiscíveis. Esse método consiste em
deixar a mistura em repouso e o componente mais denso, sob a ação da força da
gravidade, formará a fase inferior e o menos denso ocupará a fase superior. Quando
a mistura a ser separada é constituída de dois líquidos imiscíveis, pode se
utilizar um funil de vidro, conhecido como Funil de Decantação ou Funil
de Bromo. A decantação é usada nas estações de tratamento de água, para
precipitar os componentes sólidos que estão misturados com a água.
- Centrifugação: é usado para acelerar a
decantação da fase mais densa de uma mistura heterogênea constituída de um
componente sólido e outro líquido. Esse método consiste em submeter a mistura a
um movimento de rotação intenso de tal forma que o componente mais denso se
deposite no fundo do recipiente. A manteiga é separada do leite por
centrifugação. Como o leite é mais denso que a manteiga, formará a fase
inferior. Nos laboratórios de análise clínica o sangue, que é uma mistura
heterogênea, é submetido a centrifugação para separação dos seus componentes. A
centrifugação é utilizada na máquina de lavar roupa, na separação da água e do
tecido que constitui a roupa.
- Filtração: é usada para separação de
misturas heterogêneas, constituídas de um componente sólido e outro líquido ou
de um componente sólido e outro gasoso. A mistura deve passar através de um
filtro, que é constituído de um material poroso, e as partículas de maior
diâmetro ficam retidas no filtro. Método utilizado no aspirador de pó.
- Evaporação: é usado para separação de
misturas homogêneas constituída de um componente sólido e o outro líquido. É
usada para separar misturas, quando apenas a fase sólida é de interesse. O sal
de cozinha é extraído da água do mar por evaporação.
Ligas metálicas
Para produção de objetos,
ornamentos, utensílios domésticos muitas vezes é necessário separar os
componentes de um mistura para obtenção das substâncias puras, mas outras vezes
é necessário fazermos misturas de substâncias para obtermos alguns materiais.
Quando nessas misturas um dos componentes é um metal forma-se um liga metálica.
As ligas metálicas apresentam
características diferentes dos metais puros e por isso podem ser utilizadas com
maior vantagem em relação ao metal puro. As ligas de cobre e cromo são usadas
em resistências elétricas como a de chuveiro porque ocorre a diminuição da
condutividade elétrica, em outras ligas ocorre o aumento da resistência
mecânica, a resistência a corrosão, a ductibilidade etc.
Liga
metálica
|
Componentes
|
Característica
|
Uso
|
Latão
|
Cobre e Zinco
|
resistente à corrosão
|
navios, tubos
|
Bronze
|
Cobre e Estanho
|
resistente à corrosão
|
moedas, sinos
|
Aço
|
Ferro e carbono
|
resistente à corrosão
|
navios, utensílios domésticos
|
Aço inoxidável
|
Aço e Cromo
|
resistente à corrosão
|
talheres, utensílios domésticos
|
Aço -Níquel
|
Aço e Níquel
|
resistência mecânica
|
canhões, material de blindagem
|
Aço-Tungstênio
|
Aço e Tungstênio
|
alta dureza
|
brocas, pontas de caneta
|
Alnico
|
Aço, alumínio, níquel e cobalto
|
propriedades magnéticas
|
fabricação de imãs
|
Amálgama
|
Mercúrio, prata e estanho
|
Plasticidade, resistência
|
restauração de dentes
|
Ouro 18 quilates
|
Ouro e cobre
|
alta ductibilidade e maleabilidade
|
jóias
|
Prata de lei
|
Prata e cobre
|
aumento da dureza
|
utensílios domésticos,
ornamentos |
Electron Liga de magnésio
|
Mg, alumínio, manganês, zinco
|
resistência mecânica e térmica
|
peças muito leves
|
****************
Sistema circulatório
O coração e os vasos sanguíneos e o sangue formam o sistema cardiovascular ou circulatório. A circulação do sangue permite o transporte e a distribuição de nutrientes, gás oxigênio e hormônios para as células de vários órgãos. O sangue também transporta resíduos do metabolismo para que possam ser eliminados do corpo.
O coração
O coração de uma pessoa tem o tamanho aproximado de sua mão fechada, e bombeia o sangue para todo o corpo, sem parar; localiza-se no interior da cavidade torácica, entre os dois pulmões. O ápice (ponta do coração) está voltado para baixo, para a esquerda e para frente. O peso médio do coração é de aproximadamente 300 gramas, variando com o tamanho e o sexo da pessoa.
Observe o esquema do coração humano, existem quatro cavidades:
Átrio direito e átrio esquerdo, em sua parte superior;
Ventrículo direito e ventrículo esquerdo, em sua parte inferior.
O sangue que entra no átrio direito passa para o ventrículo direito e o sangue que entra no átrio esquerdo passa para o ventrículo esquerdo. Um átrio não se comunica com o outro átrio, assim como um ventrículo não se comunica com o outro ventrículo. O sangue passa do átrio direito para o ventrículo direito através da valva atrioventricular direita; e passa do átrio esquerdo para o ventrículo esquerdo através da valva atrioventricular esquerda.
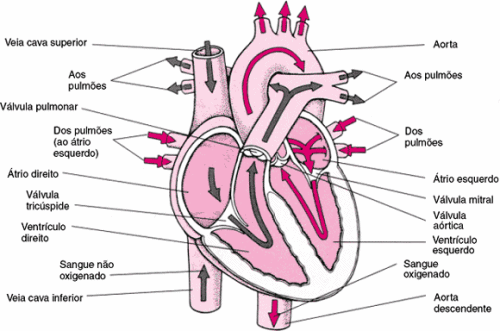
O coração humano um órgão cavitário (que apresenta cavidade), basicamente constituído por três camadas:
Pericárdio – é a membrana que reveste externamente o coração, como um saco. Esta membrana propicia uma superfície lisa e escorregadia ao coração, facilitando seu movimento ininterrupto;
Endocárdio – é uma membrana que reveste a superfície interna das cavidades do coração;
Miocárdio – é o músculo responsável pelas contrações vigorosas e involuntárias do coração; situa-se entre o pericárdio e o endocárdio.
Quando, por algum motivo, as artérias coronárias – ramificações da aorta – não conseguem irrigar corretamente o miocárdio, pode ocorrer a morte (necrose) de células musculares, o que caracteriza o infarto do miocárdio.
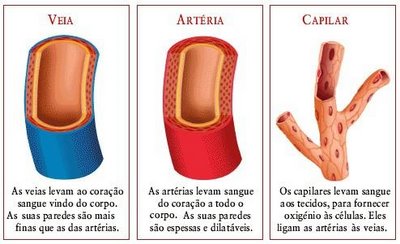
Existem três tipos básicos de vasos sanguíneos em nosso corpo: artérias, veias e capilares.
Artérias
As artérias são vasos de paredes relativamente espessa e muscular, que transporta sangue do coração para os diversos tecidos do corpo. A maioria das artérias transporta sangue oxigenado (rico em gás oxigênio), mas as artérias pulmonares transportam sangue não oxigenado (pobre em gás oxigênio) do coração até os pulmões. A aorta é a artéria mais calibrosa (de maior diâmetro) do corpo humano.
Veias
As veias são vasos de paredes relativamente fina, que transportam sangue dos diversos tecidos do corpo para o coração. A maioria das veias transporta sangue não oxigenado, mas as veias pulmonares transportam sangue oxigenado dos pulmões para o coração. As veias cavas superior e inferior são as mais calibrosas do corpo humano.
No esquema abaixo você pode ver o caminho percorrido pelo sangue em nosso corpo. Observe-o e acompanhe a explicação.
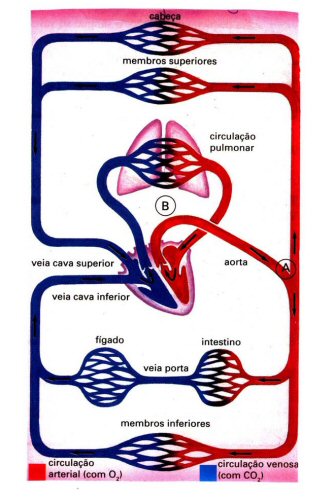
O sangue oxigenado é bombeado pelo ventrículo esquerdo do coração para o interior da aorta. Essa artéria distribui o sangue oxigenado para todo o corpo, através de inúmeras ramificações, como a artéria coronária, a artéria carótida e a artéria braquial.
Nos tecidos, o sangue libera gás oxigênio e absorve gás carbônico. O sangue não oxigenado e rico em gás carbônico é transportado por veias diversas, que acabam desembocando na veia cava superior e na veia cava inferior. Essas veias levam então o sangue não oxigenado até o átrio direito. Deste, o sangue não oxigenado passa para o ventrículo direito e daí é transportado até os pulmões pelas artérias pulmonares.
Nos pulmões, o sangue libera o gás carbônico e absorve o gás oxigênio captado do ambiente pelo sistema respiratório. Esse fenômeno, em que o sangue é oxigenado, chama-se hematose.
Então, o sangue oxigenado retorna ao átrio esquerdo do coração, transportado pelas veias pulmonares. Do átrio esquerdo, o sangue oxigenado passa para o ventrículo esquerdo e daí é impulsionado para o interior da aorta, reiniciando o circuito.
Num circuito completo pelo corpo, o sangue passa duas vezes pelo coração humano.
Nesse circuito são reconhecidos dois tipos de circulação: a pequena circulação e a grande circulação.
Pequena circulação- Também chamada circulação pulmonar, compreende o trajeto do sangue desde o ventrículo direito até o átrio esquerdo. Nessa circulação, o sangue passa pelos pulmões, onde é oxigenado.
Grande circulação- Também chamada de circulação sistêmica, compreende o trajeto do sangue desde o ventrículo esquerdo até o átrio direito; nessa circulação, o sangue oxigenado fornece gás oxigênio os diversos tecidos do corpo, além de trazer ao coração o sangue não oxigenado dos tecidos.
Pelo que foi descrito, e para facilitar a compreensão:
- A aorta transporta sangue oxigenado do ventrículo esquerdo do coração para os diversos tecidos do corpo;
- as veias cavas (superior e inferior) transportam sangue não oxigenado dos tecidos do corpo para o átrio direito do coração;
- as artérias pulmonares transportam sangue não oxigenado do ventrículo direito do coração até os pulmões;
- as veias pulmonares transportam sangue oxigenado dos pulmões até o átrio esquerdo do coração.
Observe que, pelo lado direito do nosso coração, só passa sangue não oxigenado e, pelo lado esquerdo, só passa sangue oxigenado. Não ocorre, portanto, mistura de sangue oxigenado com o não oxigenado.
A separação completa entre esses dois tipos de sangue contribui para a manutenção de uma temperatura constante no nosso organismo. Sendo os tecidos irrigados por sangue oxigenado, não “misturado” com sangue não oxigenado, nossas células recebem uma quantidade suficiente de gás oxigênio, para “queimar” uma quantidade de alimentos capaz de fornecer o calor necessário para manter mais ou menos constante a temperatura do corpo.
Faça frio, faça calor, nossa temperatura interna permanece, em condições normais, em torno de 36,5 ºC.
Vasos capilares
Os vasos capilares – muito finos (são microscópicos) e permeáveis – estão presentes nos tecidos do corpo humano, cedendo nutrientes, gás oxigênio e hormônios às células. Além disso, recolhem gás carbônico e resíduos do metabolismo celular.
Há capilares arteriais e capilares venosos. As artérias se ramificam sucessivamente, formando vasos de calibres menores chamados arteríolas. Estas continuam se ramificando e formam os capilares arteriais. Os capilares venosos, espalhados pelo nosso corpo, juntam-se até formar vênulas. As vênulas vão se unificando até formar as veias. Assim, o sangue circula em nosso organismo por um sistema fechado de vasos, pela continuidade dos capilares venosos e arteriais nos tecidos.
Como o coração funciona
Trabalhando como uma espécie de bomba, o coração se contrai e se dilata. Encostando a orelha no peito de um colega, por exemplo, você deverá ouvir facilmente as batidas do coração. A contração da musculatura do coração é chamada sístole, o relaxamento é chamado diástole. Primeiro ocorre a sístole dos átrios: o sangue passa para os ventrículos. Em seguida, ocorre a sístole dos ventrículos: o sangue é impelido para as artérias pulmonares e para a aorta. Após a sístole, ocorre a diástole da musculatura cardíaca nos átrios e nos ventrículos: os átrios se enchem de sangue e o processo da sístole recomeça.
Medindo a pressão arterial

Alternando-se ordenadamente, a sístole e a diástole são responsáveis pelo fluxo de sangue dentro dos vasos sanguíneos.
A pressão arterial que se mede é a pressão exercida pelo sangue sobre as paredes da aorta após ser lançado pelo ventrículo esquerdo. Ela é diferente na sístole e na diástole ventricular.
A pressão arterial máxima corresponde ao momento em que o ventrículo esquerdo bombeia sangue para dentro da aorta e esta se distende. Já a pressão arterial mínima é a que se verifica no final da diástole do ventrículo esquerdo.
A pressão arterial máxima corresponde a 120 mm de mercúrio, enquanto a pressão arterial mínima corresponde a 80 mm de mercúrio. Estes são os valores normais para a população. Daí falar-se em 120 por 80 ou 12 por 8 para a pressão normal.
Por meio de um aparelho chamado esfigmomanômetro, a pressão arterial pode ser medida pelo médico ou profissional habilitado. O valor da pressão arterial é um dado importante na avaliação das condições de saúde do sistema cardiovascular.
Sangue
Você já sabe que o sangue transporta nutrientes, gases respiratórios, hormônios e resíduos do metabolismo. Embora o sangue pareça um líquido vermelho completamente homogêneo, ao microscópio óptico podemos observar que ele é constituído basicamente de: plasma, glóbulos vermelhos, glóbulos brancos e plaquetas.
O plasma é a porção líquida do sangue, contém água (mais de 90%), proteínas e sais minerais diversos, glicose e vitaminas, entre outras substâncias.
Os glóbulos vermelhos
Os glóbulos vermelhos são também denominados eritrócitos ou hemácias. Veja novamente o aspecto dessas células na foto abaixo.
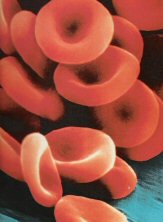
As hemácias são as mais numerosas células sanguíneas. No ser humano, existem cerca de 5 milhões delas por milímetro cúbito de sangue. Elas são produzidas na medula óssea vermelha dos ossos. Não possuem núcleo e apresentam a forma de disco côncavo em ambos os lados. A forma discóide e a concavidade em ambos os lados garantem uma superfície relativamente grande para a captação e a distribuição de gás oxigênio.
A cor vermelha das hemácias se deve à presença do pigmento hemoglobina. O gás oxigênio se combina com a hemoglobina, formando a oxiemoglobina. Nos tecidos, essa combinação é desfeita e o gás oxigênio passa para o interior das células. Assim, as hemácias promovem o transporte e a distribuição de gás oxigênio para todas as partes do corpo.
As hemácias duram cerca de 90 a 120 dias. Após esse período elas envelhecem e morrem e na própria medula óssea são repostas.
Os glóbulos brancos
Os glóbulos brancos ou leucócitos são as células de defesa do organismo que destroem os agentes estranhos, por exemplo, as bactérias, os vírus e as substâncias tóxicas que atacam o nosso organismo e causam infecções ou outras doenças. Leucócito é uma palavra composta, de origem grega, que significa “célula branca”: leuco significa “branco” e cito, “célula”.
Os leucócitos constituem o principal agente do sistema de defesa do nosso organismo, denominado também de sistema imunológico. No sangue, há de vários tipos, de diferentes formatos, tamanhos e formas de núcleo. Eles são: neutrófilos, monócitos, basófilos, eusinófilos, linfócitos.
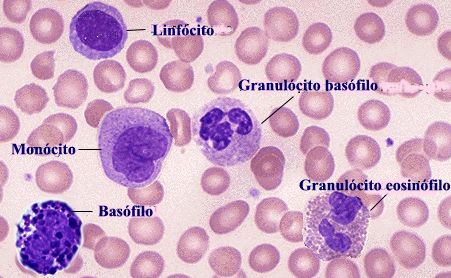
Os leucócitos são maiores que as hemácias, no entanto a quantidade deles no sangue é bem menor. Quando o organismo é atacado por vírus ou bactérias, o número de leucócitos aumenta significativamente. Atuam na defesa do organismo de dois modos:
Fagocitose – nesse processo, as células sanguíneas de defesa englobam, digerem e destroem os microrganismos invasores. Fagocitose é uma palavra composta de origem grega, formada por fago, que significa “comer, digerir”, e cito “célula”.
Produção de anticorpos – os anticorpos, proteínas especiais, neutralizam a ação das substâncias tóxicas produzidas pelos seres invasores ou presentes em alimentos e substâncias diversas.
O pus que geralmente se acumula no local de um machucado é formado pelo conjunto de leucócitos, de microrganismos mortos, e também o líquido que sai dos capilares nos pontos infectados, provocando inchaço.
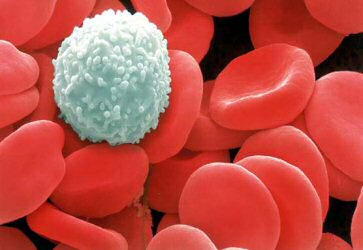
Microscopia eletrônica mostrando as hemácias (em vermelho) e um glóbulo branco (em branco).
O tempo de vida dos leucócitos ou glóbulos brancos varia. Em período de intensa atuação em defesa do organismo, duram horas e até dias.
Anticorpos, vacinas e soros
As vacinas são produtos constituídos por microorganismos mortos ou atenuados (enfraquecidos) ou, ainda, por toxinas produzidas por esses microorganismos inativadas em laboratório. Assim, as vacinas contêm antígenos incapazes de provocar a doença, mas capazes de induzir o nosso organismo a produzir anticorpos, Dessa forma, se o indivíduo, depois de vacinado, entrar em contato com esses microrganismos, o corpo já terá anticorpos suficientes para sua defesa.
É importante que todas as crianças sejam vacinadas segundo recomendações médicas. Nos postos de saúde são aplicadas vacinas contra muitas doenças, como a tuberculose, o tétano, a difteria, a coqueluche, o sarampo e a paralisia infantil. É necessário que os pais levem seus filhos para tomarem as vacinas na época certa. Quando tomadas adequadamente, as vacinas imunizam a pessoa contra às doenças as quais se destinam.
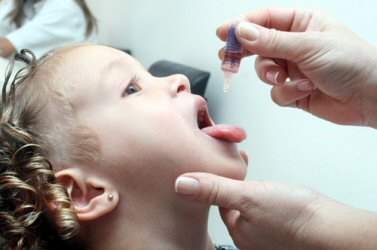
Entretanto, o corpo de uma pessoa pode ser invadido por um microorganismo contra o qual ainda não está protegido. Suponha que a ação desse microorganismo seja rápida e devastadora e que a pessoa não tenha tempo hábil para produzir anticorpos. Nesse caso, é preciso que a pessoa receba o soro terapêutico, que já contém os anticorpos necessários à inativação dos antígenos.
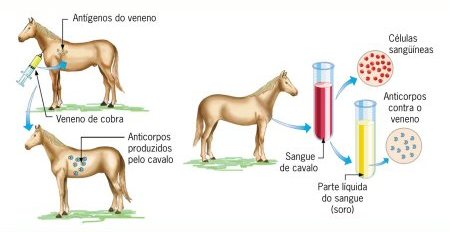
A ciência moderna dispõe de soros terapêuticos contra a ação de toxinas produzidas por certos microorganismos (exemplo: soro antitetânico, que combate o tétano, doença causada por um tipo de bactéria), e também contra toxinas presentes no veneno de certos animais, como cobras peçonhentas (soro antiofídico). Assim, enquanto as vacinas contêm antígenos e induzem o organismo a produzir anticorpos, os soros já contêm anticorpos prontos. As vacinas, graças às “células de memória”, que podem garantir uma imunidade duradoura; os soros curam a doença, proporcionando uma proteção rápida, mas temporária.
As plaquetas
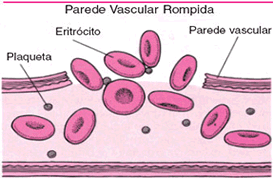
As plaquetas são fragmentos celulares bem menores que as células sanguíneas, ou seja, menores que as hemácias e os leucócitos. As plaquetas atuam na coagulação do sangue. Quando há um ferimento com rompimento do vaso sanguíneo, ocorre uma série de eventos que impedem a perda de sangue.
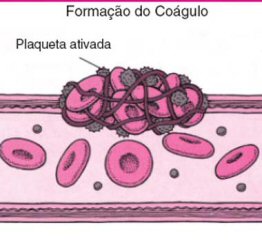
A coagulação ou formação de coágulo, que faz parte desse processo, se dá quando filamentos de uma proteína do plasma transformada, formam uma espécie de rede e impedem a passagem do sangue. O coágulo evita hemorragia, isto é, a perda de sangue que pode ocorrer na superfície do corpo – por exemplo, na pele do braço ou da mão – ou nos órgãos internos, como estômago e intestino. À medida que o vaso sanguíneo vai se cicatrizando, o coágulo seca e é reabsorvido pelo organismo.
Os grupos sanguíneos
O fornecimento seguro de sangue de um doador para um receptor requer o conhecimento dos grupos sanguíneos. Estudaremos dois sistemas de classificação de grupos sanguíneos na espécie humana: os sistemas ABO e Rh. Nos seres humanos existem os seguintes tipos básicos de sangue em relação aos sistema ABO: grupo A, grupo B, grupo AB e grupo O.
Cada pessoa pertence a um desses grupos sanguíneos. Nas hemácias humanas podem existir dois tipos de proteínas: o aglutinogênio A e o aglutinogênio B. De acordo com a presença ou não dessas hemácias, o sangue é assim classificado:
- Grupo A – possui somente o aglutinogênio A;
- Grupo B – possui somente o aglutinogênio B;
- Grupo AB – possui somente o aglutinogênio A e B;
- Grupo O – não possui aglutinogênios.
No plasma sanguíneo humano podem existir duas proteínas, chamadas aglutininas: aglutinina anti-A e aglutinina anti-B.
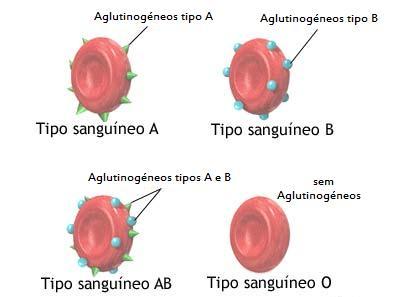
Se uma pessoa possui aglutinogênio A, não pode ter aglutinina anti-A, da mesma maneira, se possui aglutinogênio B, não pode ter aglutinina anti-B. Caso contrário, ocorrem reações que provocam a aglutinação ou o agrupamento de hemácias, o que pode entupir vasos sanguíneos e comprometer a circulação do sangue no organismo. Esse processo pode levar a pessoa à morte.
Na tabela abaixo você pode verificar o tipo de aglutinogênio e o tipo de aglutinina existentes em cada grupo sanguíneo:
Grupo sanguíneo
|
Aglutinogênio
|
Aglutinina
|
A
|
A
|
anti-B
|
B
|
B
|
anti-A
|
AB
|
A e B
|
Não possui
|
O
|
Não possui
|
anti-A e anti-B
|
A existência de uma substância denominada fator Rh no sangue é outro critério de classificação sanguínea. Diz-se, então, que quem possui essa substância no sangue é Rh positivo; quem não a possui é Rh negativo. O fator Rh tem esse nome por ter sido identificado pela primeira vez no sangue de um macaco Rhesus.
A transfusão de sangue consiste em transferir o sangue de uma pessoa doadora para outra receptora. Geralmente é realizada quando alguém perde muito sangue num acidente, numa cirurgia ou devido a certas doenças.
Nas transfusões de sangue deve-se saber se há ou não compatibilidade entre o sangue do doador e o do receptor. Se não houver essa compatibilidade, ocorre aglutinação das hemácias que começam a se dissolver (hemólise). Em relação ao sistema ABO, o sangue doado não deve conter aglutinogênios A; se o sangue do receptor apresentar aglutininas anti-B, o sangue doado não pode conter aglutinogênios B.
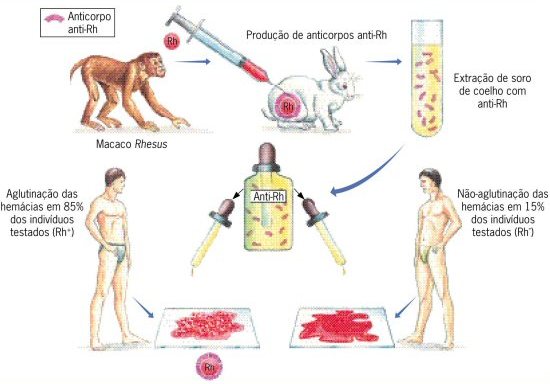
Em geral os indivíduos Rh negativos (Rh-) não possui aglutininas anti-Rh. No entanto, se receberem sangue Rh positivo (Rh+), passam a produzir aglutininas anti-Rh. Como a produção dessas aglutininas ocorre de forma relativamente lenta, na primeira transfusão de sangue de um doador Rh+ para um receptor Rh-, geralmente não há grandes problemas. Mas, numa segunda transfusão, deverá haver considerável aglutinação das hemácias doadas. As aglutininas anti-Rh produzidas dessa vez, somadas as produzidas anteriormente, podem ser suficientes para produzir grande aglutinação nas hemácias doadas, prejudicando os organismos.
O sistema linfático
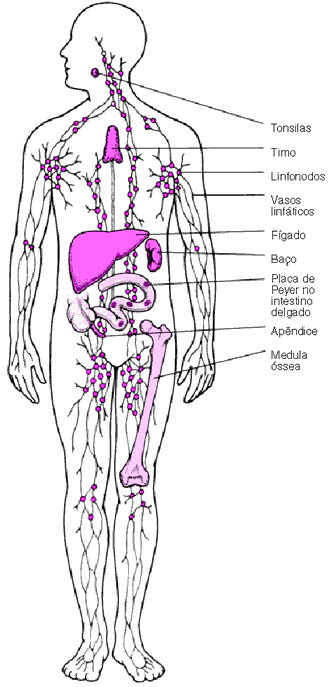
Além do sistema cardiovascular (circulatório) para a circulação do sangue, o corpo humano possui outro sistema de fluxo de líquido: o sistema linfático.
O sistema linfático compreende o conjunto formado pela linfa, pelos vasos linfáticos e órgãos como os linfonodos, o baço, o timo e as tonsilas palatinas. A linfa é um líquido claro, ligeiramente amarelado, que flui lentamente em nosso corpo através dos vasos linfáticos. Parte do plasma sanguíneo extravasa continuamente dos vasos capilares, formando um material líquido entre as células dos diversos tecidos do organismo – o líquido intercelular ou intersticial.
Uma parte desse líquido intercelular retorna aos capilares sanguíneos, carregando gás carbônico e resíduos diversos. Outra parte – a linfa – é recolhida pelos capilares linfáticos. Os capilares linfáticos transportam a linfa até vasos de maior calibre, chamados vasos linfáticos. Esses vasos semelhantes às veias, por sua vez, desembocam em grandes veias, onde a linfa é liberada, misturando-se com o sangue. Ao longo do seu trajeto, os vasos linfáticos passam pelo interior de pequenos órgãos globulares, chamados linfonodos. Os vasos linfáticos passam ainda por certos órgãos, como as tonsilas palatinas (amídalas) e o baço.
O sistema linfático não possui um órgão equivalente ao coração. A linfa, portanto, não é bombeada como no caso do sangue. Mesmo assim se desloca, pois as contrações musculares comprimem os vasos linfáticos, provocando o fluxo da linfa.
Os vasos linfáticos possuem válvulas que impedem o refluxo (retorno) da linfa em seu interior: assim, ela circula pelo vaso linfático num único sentido. O sistema linfático auxilia o sistema cardiovascular na remoção de resíduos, na coleta e na distribuição de ácidos graxos e gliceróis absorvidos no intestino delgado e contribui para a defesa do organismo, produzindo certos leucócitos, como os linfócitos.
Fonte: Só Biologia
xxxxxxxxxxxxxxxxxxxxxxxxxxxxx
Sistema Respiratório
O sistema respiratório fornece oxigênio e remove gás carbônico do organismo, auxiliando as células no metabolismo, atuando em conjunto com o sistema circulatório. O sistema respiratório também esta envolvido com a vocalização.
É formado pelo nariz, cavidade do nariz, faringe, laringe, traquéia, brônquios e pulmões.
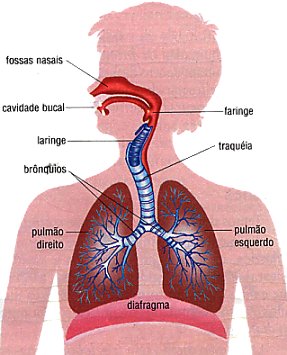
Nariz e cavidade do nariz
As duas cavidades por onde o ar entra no sistema respiratório são chamadas de fossas nasais. São separadas por uma cartilagem chamada cartilagem do septo, formando o septo nasal. Os pêlos no interior do nariz retém as partículas que entram junto com o ar. É composto de células ciliadas e produtoras de muco. O teto da cavidade nasal possui células com função olfativa. Nesta região, a mucosa é bem irrigada e aquece o ar inalado.
Faringe
A faringe pertence tanto ao sistema respiratório como ao sistema digestório. Através das coanas esta ligada com a cavidade do nariz e através das fauces, com a boca. Liga-se com o ouvido médio pelas tubas auditivas. Liga-se também com a laringe e com o esôfago. Antes de ir para a laringe, o ar inspirado pelo nariz passa pela faringe.
Laringe
A laringe é um tubo cartilaginoso de forma irregular que conecta a faringe com a traquéia. Situa-se na parte superior do pescoço. A laringe possui uma estrutura cartilaginosa que chama epiglote, que trabalha para desviar das vias respiratórias para o esôfago os alimentos deglutidos. Caso não ocorra este desvio, o alimento é expelido com uma tosse violenta.
Na laringe encontramos as cordas vocais, que são pregas horizontais na parede da laringe. Entre as cordas vocais há uma abertura chamada glote e é por ela que o ar entra na laringe, provocando uma vibração nas cordas vocais e produzindo som. Na face anterior do pescoço forma-se a proeminência laríngea, chamada de pomo de Adão, que é mais visível nos homens que nas mulheres.
Traquéia
A traquéia é um tubo de aproximadamente 12 cm de comprimento e 2,5 de diâmetro e suas paredes são reforçadas por uma série de anéis de cartilagem que impedem que as paredes se colapsem.
A traquéia bifurca-se na sua região inferior, originando os brônquios.
O epitélio é formado por células ciliadas e células secretoras. Estes cílios servem para remover as partículas e microorganismos que entram com o ar inalado. O muco produzido pelas células secretoras serve como uma barreira também.
Pulmão
Os brônquios penetram no pulmão através do hilo. Esses brônquios ramificam-se várias vezes, originando os bronquíolos, que penetram no lóbulo pulmonar e ramificam-se, formando os bronquíolos terminais, que originam os bronquíolos respiratórios, que terminam nos alvéolos pulmonares.
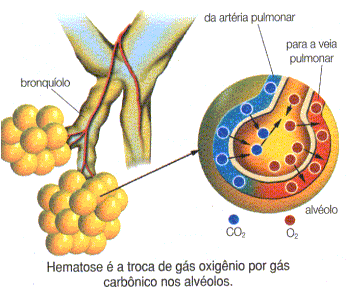
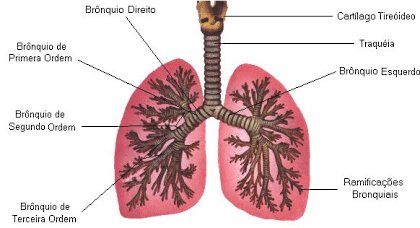
Os pulmões possuem consistência esponjosa, que está relacionada com a quantidade de sacos alveolares.
O formato do pulmão lembra um cone e é revestido por uma membrana dupla serosa chamada pleura. Os dois pulmões são separados pelo mediastino, local onde está o coração, o esôfago, timo, artérias, veias e parte da traquéia.
O diafragma é um músculo situado abaixo do pulmão, e é onde ele se apóia. Separa o tórax do abdome e está relacionado com os movimentos da respiração.
No mundo todo, as doenças que acometem o sistema respiratório ocupam o posto de terceira causa de morte. Dentre as doenças mais comuns que acometem o aparelho respiratório estão:
Os pulmões são órgãos que compõem o sistema respiratório, responsáveis pelas trocas gasosas entre o ambiente e a corrente sanguínea. São dois órgãos de formato piramidal, sendo estes os principais órgãos do sistema respiratório dos humanos.
As doenças mais comumente observadas que acomete os pulmões são:
Doença pulmonar obstrutiva crônica (DPOC);
Bronquite crônica;
Enfisema pulmonar;
Asma;
Câncer de pulmão.
Doença Pulmonar Obstrutiva Crônica
Esta é uma doença crônica, progressiva e irreversível que afeta os pulmões, apresentando como principal característica a destruição de muitos alvéolos pulmonares e o comprometimento dos restantes. É mais comum em indivíduos do sexo masculino com idade avançada, sendo que também é frequente sua observação em indivíduos que já tiveram tuberculose.
Os principais fatores que levam ao aparecimento da DPOC relacionam-se ao tabagismo, vindo em seguida o fumo passivo, exposição à poeira por longos anos, poluição do ambiente e, em certos casos, fatores genéticos.
De acordo com dados da Organização Mundial de Saúde (OMS), aproximadamente 80 milhões de pessoas apresentam DPOC moderada a severa, No Brasil, esta afecção acomete em torno de 5,5 milhões de pessoas por ano, segundo o Conselho Brasileiro de DPOC.
Normalmente os pacientes com DPOC apresentam sintomatologia tanto da bronquite crônica quanto do enfisema pulmonar. Deste modo, atualmente utiliza-se mais o termo DPOC quando se faz referência a bronquite crônica e enfisema pulmonar, uma vez que, normalmente, as mesmas coexistem no mesmo paciente apresentando obstrução do fluxo de ar.
Bronquite Crônica
A bronquite crônica é definida como uma inflamação dos brônquios. Geralmente, surge depois de 20 a 30 anos de exposição dos brônquios a fatores irritantes, como o tabaco, poluição do ar, entre outras fontes. Sua ocorrência é mais comum em mulheres do que em homens.
Esta afecção pode preceder ou acompanhar o enfisema pulmonar.
Enfisema Pulmonar
Esta é uma doença crônica, na qual ocorre destruição gradativa dos tecidos pulmonares, passando estes a ficarem hiperinsuflados. Normalmente sua etiologia reside na exposição prolongada ao tabaco ou produtos químicos tóxicos.
Asma
A asma, também conhecida como asma brônquica ou bronquite asmática, é uma afecção pulmonar caracterizada pela inflamação das vias aéreas, que leva à diminuição ou até mesmo obstrução do fluxo de ar. Sua fisiopatologia está ligada a fatores genéticos e ambientais, manifestando-se por meio de crises de falta de ar.
Nos Estados Unidos, essa doença leva ao óbito aproximadamente 5% dos adultos. Tanto os internamentos quanto os óbitos relacionados a essa doença tem aumentado. No Brasil, dentro do SUS, a asma representa a terceira causa de internamentos, sendo que no ano de 2007 foram registradas 273.205 internações por essa doença no Brasil (2,41% das internações totais).
Câncer de Pulmão
O câncer de pulmão é um dos tumores malignos mais comuns, sendo que sua incidência no mundo todo vem aumentando 2% a cada ano. A mortalidade por esse tipo de neoplasia é muito elevada e o prognóstico está relacionado à fase em que é diagnosticado.
O principal fator de risco para o aparecimento dessa neoplasia é o tabagismo. Atualmente, este último corresponde a 90% dos casos desse tumor. É mais comumente observado em homens do que em mulheres; todavia, o número de casos em mulheres está aumentando, enquanto que o número de casos em homens está diminuindo.
Esta neoplasia também pode ser causada por certos produtos químicos, como: arsênico, berílio, asbesto, radônio, níquel, cromo, cádmio e cloreto de vinila, especialmente observados em ambiente ocupacional. Outros fatores relacionados ao surgimento desse tumor são os dietéticos, genéticos, histórico da DPOC e histórico de câncer de pulmão na família.
Fonte: http://www.infoescola.com
+++++++++++++++++++++++++++++Sistema Digestório
link da apresentação:
https://drive.google.com/file/d/0B4YOME2XSxFHbXZHU2hrak1DM0U/edit?usp=sharing
============================
Alguns sites que vão ajudar nos trabalhos de pesquisa sobre vantagens adaptativas das flores para as Angiospermas - 7EF
(página 13 do livro, principalmente 1º e 2º parágrafos)
Pizza 3º ano - Julho 2014
Seguem aí as lâminas da apresentação. Bom estudo!
HISTOLOGIA - 8EF
Definições
ØConjunto de células que atuam de maneira integrada, desempenhando determinadas funções.
ØO Ramos da Biologia que estuda os tecidos e as células que os formam é a Histologia (histo = tecido; logia = estudo).
ØOs tecidos animais podem ser classificados em quatro tipos principais:
ØTecidos epiteliais;
ØTecidos conjuntivos;
ØTecidos musculares;
ØTecido nervoso.
Tecidos epiteliais
ØOs tecidos epiteliais, ou simplesmente epitélios, são formados por células justapostas, firmemente unidas entre si, com pouca substância entre elas (substância intercelular).
Ø Reveste e protege as superfícies do organismo.
Ø Geralmente têm formato poliédrico (cúbicas, cilíndricas, etc.).
Ø Encontradas nos alvéolos pulmonares, vasos sanguíneos e linfáticos, túbulos renais, estômago e intestinos, cavidade nasal, traquéia, brônquios; em áreas de atrito como pele, mucosas bucal e vaginal; bexiga urinária e glândulas.
Ø(foto: epitélio nasal)
Pele
Ø A pele é um dos órgãos do nosso corpo. A parte superficial é conhecida como epiderme, formada por várias camadas de tecido epitelial. A parte mais profunda é chamada de derme, formada de tecido conjuntivo.
Ø representa cerca de 15% do peso de um ser humano, cobrindo ma área aproximada de 2m2.
Ø presença de queratina e melanina.
Ø as células epiteliais têm vida curta e precisam ser constantemente renovadas. A velocidade de renovação varia de epitélio para epitélio. Epitélio intestinal: 2 a 5 dias; pâncreas: ~50 dias; pele: ~30 dias. No couro cabeludo pode ocorrer uma disfunção em que a descamação de parte da epiderme acontece a cada 3 ou 4 dias, formando as caspas.
ØMetaplasia: substituição patológica de um tipo de tecido por outro, alterando suas funções. Ex. fumantes.
Ø(imagem: corte de pele em diferentes regiões do corpo).
Tecido conjuntivo
ØCaracterizam-se morfologicamente por apresentarem diversos tipos de células imersas em grande quantidade de material extracelular ou matriz, constituída principalmente de água e de fibras de proteína.
ØOs diferentes tipos de tecido conjuntivo estão amplamente distribuídos pelo corpo, podendo desempenhar funções de preenchimento de espaços entre órgãos, função de sustentação, defesa , sustentação e nutrição.
ØA classificação desses tecidos baseia-se na composição de suas células e na proporção relativa entre os elementos da matriz extracelular. Alguns tipos: cartilaginoso, adiposo, ósseo e sanguíneo.
Tecido conjuntivo cartilaginoso
ØApresenta consistência firme, mas não é rígido como o tecido ósseo.
ØTem função de sustentação, reveste superfícies articulares facilitando os movimentos e é fundamental para o crescimento de ossos longos.
ØNas cartilagens não há nervos nem vasos sanguíneos. A nutrição é feita a partir dos vasos sanguíneos do tecido conjuntivo adjacente.
ØÉ encontrada no nariz, anéis da traquéia e dos brônquios, orelha externa, epiglote e em algumas partes da laringe. É muito abundante no feto, formando o esqueleto inicial que depois é substituído por tecido ósseo.
ØImagens : esquerda→ nariz e orelha; direita→ tecido cartilaginoso visto ao microscópio óptico.
Tecido conjuntivo adiposo
Ø Neste tecido a substância intercelular é reduzida, e as células, ricas em lipídios, são denominadas células adiposas.
Ø Ocorre principalmente sob a pele, exercendo funções de reserva de energia, proteção contra choques mecânicos e isolamento térmico.
Ø Ocorre também ao redor de alguns órgãos, como os rins e o coração.
ØImagens: à esquerda um esquema de células adiposas; à direita imagem de microscópio óptico de tecido adiposo. Note que as linhas são as delimitações das células e os pontos roxos são os núcleo dos adipócitos. A parte clara, parecendo um espaço vazio, é a parte da célula contendo gordura.
Tecido conjuntivo ósseo
ØTem a função de sustentação, e ocorre nos ossos do esqueleto dos vertebrados.
ØÉ um tecido rígido graças à presença de substância fundamental rica em sais de cálcio, fósforo e magnésio. Além desses elementos, a matriz é rica em fibras colágenas, que fornecem certa flexibilidade ao osso.
ØOs ossos são ricos em vasos sanguíneos e nervos, apresentando sensibilidade, alto metabolismo e capacidade de regeneração.
ØO interior dos ossos é preenchido pela medula óssea, que pode ser de dois tipos: amarela, constituída por tecido adiposo, e vermelha, formadora de células do sangue.
ØApesar de ser um órgão duro e resistente, é capaz de remodelar sua estrutura interna em resposta a modificações nas forças a que está normalmente submetido. Ex.: aparelhos ortodônticos, que remodelam a arcada dentária.
Tecido sanguíneo ou reticular ou hemocitopoético
ØÉ um tipo de tecido conjuntivo em que a substância extracelular é líquida e constitui o plasma sanguíneo, formado principalmente de água.
ØO sangue possui diferentes tipos de células: glóbulos vermelhos (eritrócitos ou hemácias), glóbulos brancos (ou leucócitos), plaquetas (ou trombócitos).
ØNo corpo humano o sangue transporta nutrientes, gases respiratórios (O2 e CO2), hormônios e resíduos da atividade celular, como a uréia, que devem ser eliminados do organismo. Participa também da defesa do organismo por meio da ação dos glóbulos brancos.
ØImagem: observa-se componentes do sangue visto em microscópio eletrônico (glóbulos vermelhos e um glóbulo branco)
Tecido muscular
ØRelacionam-se com a locomoção e outros movimentos do corpo, como a contração dos órgãos do tubo digestório, do coração e das artérias.
ØAs células dos tecidos musculares são alongadas e recebem o nome de fibras musculares ou miócitos; possuem capacidade de contração e relaxamento.
ØHá 3 tipos de tecido muscular: estriado esquelético, estriado cardíaco e liso ou não estriado.
Tecido muscular estriado esquelético
Øcontração vigorosa e voluntária, isto é, contraem-se de acordo com a nossa vontade. Ex.: peitoral maior, bíceps e tríceps braquial.
ØPermitem o movimento dos diversos ossos e cartilagens do esqueleto.
Tecido muscular estriado cardíaco
Øesse tecido ocorre apenas no coração e apresenta contração independente da vontade do indivíduo (contração involuntária).
ØEsse tecido constitui o miocárdio, o músculo do coração.
ØSuas células são menores e ramificadas, intimamente unidas entre si.
ØImagem: coração humano retirado para análise laboratorial.
Tecido muscular liso ou não-estriado
Øpossui um conjunto de células com contração involuntária e lenta.
ØOcorre nas artérias; esôfago, estômago e intestino; bexiga urinária e outros órgãos.
ØPossuem uma boa capacidade de regeneração.
Tecido nervoso
ØO tecido nervoso participa da constituição dos órgãos que formam o sistema nervoso, como o cérebro.
ØOs neurônios, ou células nervosas, têm a propriedade de receber e transmitir estímulos nervosos, permitindo ao organismo responder a alterações do meio. São células formadas por um corpo celular, de onde partem dois tipos de prolongamentos: dendritos e axônio.
ØOs dendritos são prolongamentos ramificados da célula especializados em receber estímulos. O impulso nervoso é sempre transmitido no sentido dendrito→ corpo celular → axônio.
ØO axônio é uma expansão da célula com ramificações em sua porção final. É uma estrutura especializada na transmissão de impulsos nervosos para outros neurônios.







































Nenhum comentário:
Postar um comentário